Hjem » Hepato-gastro-enterologisk patofysiologi » Refeeding syndrom
Refeeding syndrom
I Band of Brothers (serien om en gruppe amerikanske soldater, der befrier Vesteuropa under 2. verdenskrig) er der et afsnit, hvor soldaterne opdager en koncentrationslejr, hvor der fortsat er levende fanger. De er svært udhungrede og afmagrede, men sanitetstjenesten vil ikke give dem mad. Serien siger det ikke, men grunden til det er refeeding syndrom.
Og på sin vis er serien helt historisk korrekt, for refeeding syndrom blev første gang beskrevet i slutningen af krigen. For eksempel hos ofre for den store hollandske hungersnød 1944-1945 og hos japanske krigsfanger, som et hyppigt citeret studie fra 1951 handler om.
I et internationalt perspektiv er det, desværre, stadig relevant at kende til problemerne forbundet med at begynde at spise efter at have oplevet hungersnød eller fangenskab. I en dansk kontekst er det heldigvis primært på hospitalerne, man møder problemet.
Der findes flere udmærkede kilder til refeeding syndrom, og jeg har haft mest gavn af at læse artikler af Martin Crook, der har skrevet om refeeding i hvert fald i 20 år.
Et godt sted at starte er hans (og kollegers!) “The importance of the refeeding syndrome” fra 2001, hvis man kan finde den, og så kan man fortsætte med denne lidt nyere.
Dansk Selskab for Klinisk Ernæring udgav i medio maj 2023 en klinisk retningslinje, som også kunne være et godt sted at starte.
På trods af mange fine review-artikler, har jeg ikke rigtig fundet dén gode artikel, der primært beskæftiger sig med patofysiologien bag refeeding. Artiklerne angiver typisk blot korrelationer (fx ved refeeding der optræde tiaminmangel) uden at angive kausale sammenhænge. Og en del i øvrigt spændende spørgsmål lades ubesvarede, fx: hvilken mekanisme vedligeholder for eksempel plasmakoncentrationen af fosfat selv når den (formodede) intracellulære koncentration er lav? Så sidder du med et godt review eller et spændende studie, modtager jeg gerne.
Definition af refeeding syndrom
Refeeding syndrom opstår i forlængelse af opstart af ernæringsterapi efter at kroppen har været i en langvarig katabol tilstand og består i:
- En samling af elektrolytforstyrrelser, herunder
- hypomagnesiæmi
- hypofosfatæmi
- hypokaliæmi
Og/eller
- kliniske symptomer, herunder
- ødemer
- hjertesvigt
- respirationssvigt
I klinisk og forskningsmæssig praksis bliver det operationaliseret lidt forskelligt. Et review af litteraturen af Friedli et al. (2016) finder temmelig mange studier, der beskæftiger sig med refeeding, og her bruges både plasmakoncentrationen af fosfat (og vidt forskellige koncentrationer!) alene, kliniske symptomer alene og kliniske symptomer i kombination med P-fosfat som definition.
Det er ikke mærkeligt, at en artikel, også af Crook (2014), hed: Refeeding syndrome: Problems with definitions […].
For alle praktiske (dvs. kliniske) formål kan man nok tillade sig at være lidt ligeglad. Hvis patienten får elektrolytforstyrrelser, og herunder navnlig fald i P-fosfat, i takt med genoptagelse af ernæring uanset om det foregår parenteralt, gennem et plastikrør ned i maven eller gennem et spiserør ned i maven, så har du at gøre med refeeding syndrom, og så skal du gøre noget.
Patofysiologiske grundmekanismer bag refeeding syndrom
Det følgende baserer sig på Crook (2014) og Crook (2001) og hvad forfatteren selv kan trække ud af ærmet fra undervisningen i medicinsk biokemi.
Når man sulter overgår metabolismen fra en grundlæggende anabol tilstand til en grundlæggende katabol tilstand. Insulinspejlet falder og glukagonspejlet stiger, sådan at glykolysen og glykoneogenesen igangsættes. Kroppen begynder at brænde fedt og muskel og kropsvægten falder.
Samtidig depleteres intracellulære ioner, i særdeleshed fosfat, kalium og magnesium. Den (manglende) eksogene tilførsel kan ikke kompensere for de kontinuerlige, fysiologiske gastrointestinale og renale tab. Fordi der er tale om intracellulære ioner, kan plasmakoncentrationerne af ionerne principielt være helt normale på trods af depletionen.
Opstart af ernæring, uanset type, betyder tilførsel af kulhydrater og tilførsel af kulhydrater betyder insulinsekretion og et for den sultende patient et nærmest tektonisk skifte fra katabolisme til anabolisme. Det kan illustreres med nedenstående figur:
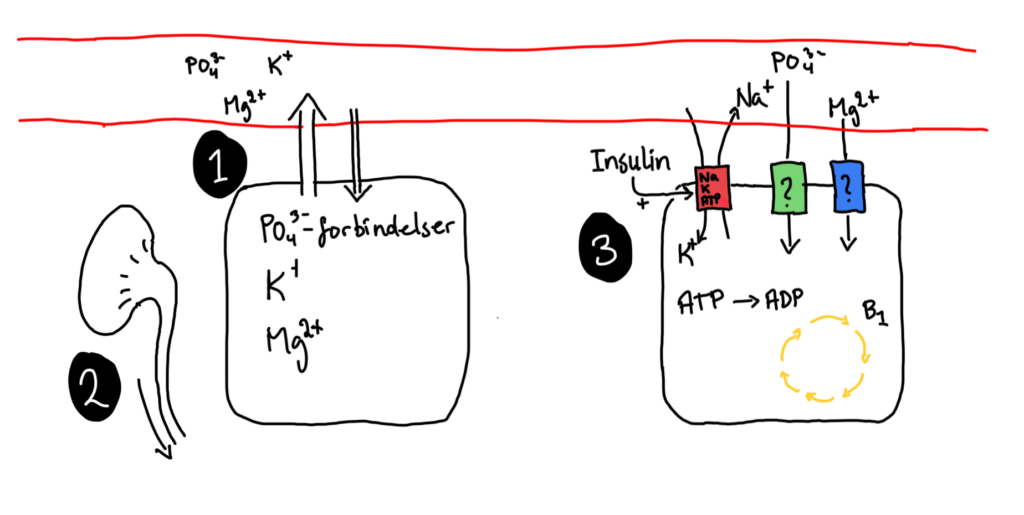
Insulinsekretion stimulerer det cellulære optag af glukose, fosfat (gennem en mekanisme, som man formentlig ikke kender til), kalium (NaKATPasen er insulinsensitiv) og magnesium (igen gennem en mekanisme, jeg ikke kender til) og giver derfor pludseligt et ekstracellulært fald, der kan måles som faldende plasmakoncentrationer.
Tiamin (B1) er en cofaktor i flere intracellulære metaboliske pathways. Det er fx en cofaktor for pyruvat dehydrogenase i omdannelsen af mitokondriel pyruvat til acetyl-coenzym A, der indgår i citratcyklus. Tiamin kan som følge af underernæring også være lavt og et øget forbrug lede til tiaminmangel.
Hypofosfatæmi ved refeeding syndrom
Er du interesseret i fosfat og cellulær fosfathomøostase kunne et godt sted at starte være Hernando et al. (2021), gratis tilgængelig hos all-time-favorite American Journal of Physiology.
Fosfat udgør 1 % af kroppen, og kun 1 % heraf er ekstracellulært beliggende og tilgængelig for intravaskulær sampling. Det er en essentiel byggesten for et utal af kropslige funktioner: Knogle– og tandmineralisering, det er rygraden i nukleinsyrerne, det er dén centrale komponent i den lettilgængelige intracellulære energipulje ATP, GTP, det findes som fosfolipider i cellemembranen, er et centralt reguleringsmolekyler af proteinfunktion som phosphoproteiner og det regulerer oxygendissociationen fra hæmoglobin.
En typisk nedre laboratorieværdi for fosfat og dermed definitorisk for hypofosfatæmi (her helt tilfældigt valgt værdier for kvinder):
- Hypofosfatæmi = P-fosfat < 0,71 mM
Der er ikke helt rigtig enighed om, hvad der konstituerer hypofosfatæmi ved refeeding. De artikler i Friedli et al. (2016), der operationaliserede refeeding syndrom udelukkende ved hjælp af P-fosfat, brugte for eksempel:
- Refeeding defineret ved hypofosfatæmi = P-fosfat < 0,50 mM
- Refeeding defineret ved hypofosfatæmi = P-fosfat < 0,87 mM
- Refeeding defineret ved hypofosfatæmi = P-fosfat-fald på ≥ 0,15 mM til P-fosfat < 0,8 mM
Med andre ord: Er der hypofosfatæmi i forbindelse med genoptag af ernæring efter længere tids abstinens, så er der refeeding syndrom (NB! det kan der også være uden hypofosfatæmi!)
De kliniske symptomer ved hypofosfatæmi opstår fra flere forskellige organsystemer og er grundlæggende uspecifikke og er en konsekvens af det nedsatte intracellulære ATP-niveau.
Generelt er kliniske symptomer ikke almindeligt ved P-fosfat > 0,32 mM, så hypofosfatæmi ved refeeding er grundlæggende et subklinisk og paraklinisk problem.
Rhabdomyolyse. Knochel et al. forsøgte i 1970’erne at gøre hunde akut hypofostatæme efter en kronisk fase med hypofosfatæmi (først langvarig fosfatdepleterede kost, herefter hyperalimentation). I den kroniske fase var der subtil muskelskade. Hos hunde der blev fodret med rigelig fosfatberiget kost gik det udmærket, men hos hunde der blev fodret med rigelig fosfatfattig kost, fandt man på muskelbiopsier forvrængede, hæmorragiske og leukocytinfiltrerede muskelceller og kreatininkinase steg vældigt. Den er god nok, tjek selv figur 2 og 6. Specielt figur 6 til sammenligning med figur 7 er ret illustrativ.
Neuromuskulære og respiratoriske symptomer. Kramper, muskelsvaghed, muskelsvækkelse. Problemet er helt exceptionelt, når det strækker sig til vejrtrækningsmuskulaturen, herunder diaphragma. Intracellulær fosfatdepletering betyder, at ATP-lagre ikke (gen)opbygges og cellen ikke har umiddelbart tilgængelig energi.
Kardiomyopati. Af grunde, jeg ikke har undersøgt nærmere. Men givet den tværstribede mikroanatomi, mon ikke der er omtrentligt de samme processer på spil som Knochel et al. viste?
Hæmatologiske effekter. På grund af faldende 2,3-DPG, hvilket betyder en venstreforskydning af hæmoglobins iltbindingskurve: Oxygen bindes hårdere til hæmoglobin og dissocierer sværere.
Der er flere andre problemer: kramper, påvirket bevidsthedsniveau, paræstesier, osteomalaci, hæmolyse, påvirket kemotaksi for leukocytter, sænket trombocytaggregationsfunktion.
Hypokaliæmi ved refeeding syndrom
Kalium er den primære intracellulære kation, og dens høje intracellulær koncentration er helt afhængig af aktiviteten i NaKATPasen.
Ved refeeding øges den pankreatiske insulinudskillelse, og NaKATPasen er insulinfølsom. Jeg gætter på, at det er den primære mekanisme bag hypokaliæmi ved refeeding. Friedli et al. (2017) påpeger også, at den øgede intracellulære proteinsyntese med flere negativt ladede proteiner skal elektrisk afbalanceres, og at det er årsagen til hypokaliæmi.
Patienter i risiko for refeeding syndrom
Flere steder i litteraturen, i instrukser og NBV’er kan man finde nogenlunde enslydende kategorier af patienter i risiko for refeeding:
- BMI < 16 kg/m2
- 15 %’s vægttab over 3 måneder
- Intet eller sparsomt fødeindtag i 10 dage
- Lav fosfat, kalium eller magnesium før opstart af ernæring.
Og i lidt lavere risiko er patienter med lidt højere BMI (18), lidt lavere vægttab (>10 %), lidt kortere fasteperiode (5 dage). Man må også tage hensyn til den kliniske kontekst, fx komorbidt alkoholmisbrug, høj alder, cancersygdom og patienter med anoreksi.
Kilder
Crook MA, Hally V, Panteli JV. The importance of the refeeding syndrome. Nutrition. 2001 Jul-Aug;17(7-8):632-7. doi: 10.1016/s0899-9007(01)00542-1. PMID: 11448586.
Crook MA. Refeeding syndrome: problems with definition and management. Nutrition. 2014 Nov-Dec;30(11-12):1448-55. doi: 10.1016/j.nut.2014.03.026. Epub 2014 Apr 18. PMID: 25280426.
Friedli N, Stanga Z, Culkin A, Crook M, Laviano A, Sobotka L, Kressig RW, Kondrup J, Mueller B, Schuetz P. Management and prevention of refeeding syndrome in medical inpatients: An evidence-based and consensus-supported algorithm. Nutrition. 2018 Mar;47:13-20. doi: 10.1016/j.nut.2017.09.007. Epub 2017 Sep 25. PMID: 29429529.
Friedli N, Stanga Z, Sobotka L, Culkin A, Kondrup J, Laviano A, Mueller B, Schuetz P. Revisiting the refeeding syndrome: Results of a systematic review. Nutrition. 2017 Mar;35:151-160. doi: 10.1016/j.nut.2016.05.016. Epub 2016 Jun 8. PMID: 28087222.
Amanzadeh J, Reilly RF Jr. Hypophosphatemia: an evidence-based approach to its clinical consequences and management. Nat Clin Pract Nephrol. 2006 Mar;2(3):136-48. doi: 10.1038/ncpneph0124. PMID: 16932412.
Hernando N, Gagnon K, Lederer E. Phosphate Transport in Epithelial and Nonepithelial Tissue. Physiol Rev. 2021 Jan 1;101(1):1-35. doi: 10.1152/physrev.00008.2019. Epub 2020 Apr 30. PMID: 32353243.
Knochel JP, Barcenas C, Cotton JR, Fuller TJ, Haller R, Carter NW. Hypophosphatemia and rhabdomyolysis. J Clin Invest. 1978 Dec;62(6):1240-6. doi: 10.1172/JCI109244. PMID: 748377; PMCID: PMC371889.
Støving RK et al. Anorexia nervosa. Dansk Endokrinologisk Selskabs Nationale Behandlingsvejledninger. På endocrinology.dk. Tilgået d. 2/5-2023.
Jeg er blevet opmærksom på, at en arbejdsgruppe under Dansk Selskab for Klinisk Ernæring (DSKE) i maj 2023 udgav en klinisk retningslinje om Refeeding Syndrom. Jeg har ikke selv læst den grundigt, men den har fine afsnit om definitioner og patofysiologi.